7月15日,国家药品监督管理局通报了长春长生生物科技有限责任公司(下称长春长生生物科技公司)因生产存在记录造假被责令停止生产冻干人用狂犬病疫苗一事。通报称,所有涉事批次产品尚未出厂和上市销售,全部产品已得到有效控制。
(通告详细内容)
国家药品监督管理局关于长春长生生物科技有限责任公司
违法违规生产冻干人用狂犬病疫苗的通告(2018年第60号)
根据线索,国家药品监督管理局组织对长春长生生物科技有限责任公司开展飞行检查,发现该企业冻干人用狂犬病疫苗生产存在记录造假等严重违反《药品生产质量管理规范》行为。
国家药品监督管理局已要求吉林省食品药品监督管理局收回该企业《药品GMP证书》(证书编号:JL20180024),责令停止狂犬疫苗的生产,责成企业严格落实主体责任,全面排查风险隐患,主动采取控制措施,确保公众用药安全。吉林省食品药品监督管理局调查组已进驻该企业,对相关违法违规行为立案调查。国家药品监督管理局派出专项督查组,赴吉林督办调查处置工作。本次飞行检查所有涉事批次产品尚未出厂和上市销售,全部产品已得到有效控制。
国家药品监督管理局始终把人民群众用药安全放在首位,坚决贯彻落实习近平总书记“四个最严”要求,对发现的违法违规问题绝不姑息,坚决依法依规严肃查处,涉嫌构成犯罪的,一律移送公安机关予以严惩。
特此通告。
国家药品监督管理局
2018年7月15日
长春长生生物科技公司官网介绍,该公司成立于1992年,2015年资产重组后上市,上市公司长生生物(002680.sz)2017年年报内容称,据中检院的数据,该公司一类疫苗和二类疫苗的批签发量分别为577万人份和1011万人份,从批签发数量看,狂犬疫苗和水痘疫苗已经位居国内第二位。其中,主要产品冻干人用狂犬疫苗(Vero细胞)批签发数量为355万人份。
澎湃新闻(www.thepaper.cn)注意到,这并非这家疫苗生产公司首次出现疫苗生产问题,2017年11月,该企业另一个疫苗产品——百白破疫苗被原食药监总局通报在药品抽样检查中,检出其一个批次产品效价指标不符合标准规定。
不过,较早前,2018年6月8日,长春长生旗下的四价流感病毒裂解疫苗刚刚通过国家药监局生产注册申请,和华兰生物疫苗有限公司一起,成为四价流感疫苗的两家国产企业。

长春长生生物冻干人用狂犬病疫苗
涉事公司去年狂犬病疫苗批签发量达355万人份
7月15日,国家药监局发布通告称,在接到举报线索后组织人员对长春生物公司开展飞行检查,并在检查中发现该企业冻干人用狂犬病疫苗生产存在记录造假等严重违反《药品生产质量管理规范》行为,对此总局责令相关单位收回该企业药品GMP(药品生产质量管理规范)证书,并责令停产。
随后,网络传出该企业当日由负责人高俊芳签发的一份《紧急通知》,要求各省推广团队立即停止使用公司狂犬疫苗并就地封存,同时立即启动召回程序。
据每日经济新闻报道,该企业一名员工证实了上述《紧急通知》,但解释称召回行为系公司自主行为,而并非以往生产的疫苗被药监局查出问题,“我们不太清楚具体是什么样的原因,可能是出于对产品安全性方面的考虑,批量有多大也不太清楚”。
上市公司长生生物发布的2017年年报显示,该公司在售一类疫苗和二类疫苗共有6个品种,疫苗种类和销售数量、销售额均稳居国内民营疫苗企业前列。
该公告还援引中检院的数据称,2017年公司一类疫苗和二类疫苗的批签发量分别为577万人份和1011万人份,其中公司主要产品冻干人用狂犬疫苗(Vero细胞)、冻干水痘减毒活疫苗、流行性感冒裂解疫苗、冻干甲型肝炎减毒活疫苗的批签发数量分别为355万人份、360万人份、257万人份、 272万人份,从批签发数量看,狂犬疫苗和水痘疫苗已经位居国内第二位。
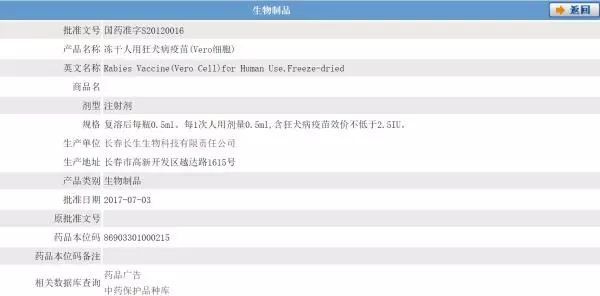
长生生物冻干人用狂犬病疫苗(Vero细胞)的药品注册信息 来源:国家药监局网站
百白破疫苗曾被通报效价不合格
根据公司官网信息,长春长生生物科技有限责任公司(前身为长春长生生物科技股份有限公司)创立于1992年8月18日,是一家从事人用疫苗研发、生产、销售的国家高新技术企业。
2015年,长生生物通过资产重组在深圳证券交易所上市,上市公司今年4月25日发布的《2018年第一季度报告》显示,公司第一季度营业总收入3.46亿,同比增长54.05%,净利润1.58亿,同比增长72.22%
长生生物并非第一次因疫苗质量问题被国家药监局通报。

长春长生生物科技有限公司生产的批号为201605014-01的百白破疫苗效价指标不符合标准规定。 来源:原国家食药监总局网站
2017年11月3日,原国家食药监总局发布了百白破疫苗效价指标不合格产品处置情况介绍,称在药品抽样检验中检出长春长生生物科技有限公司生产的批号为201605014-01的百白破疫苗效价指标不符合标准规定。
与长生生物该批次百白破疫苗一同被检出效价指标不符合标准规定的,还有武汉生物制品研究所有限责任公司生产的批号为201607050-2的百白破疫苗。
据中国疾病预防控制中心介绍,百白破疫苗是预防百日咳、白喉、破伤风的有效手段。上述通报称,长生生物生产的该批次疫苗共计25.26万支,全部销往山东省疾病预防控制中心。
随后,11月5日,中国疾病预防控制中心网站发布《效价指标不合格的百白破疫苗相关问题解答》称,该两批次百白破疫苗效价指标不合格,可能影响免疫保护效果。
不过,针对此事,长生生物曾发布公告称,该批次25.26万支百白破疫苗共实现销售收入约83.38万元,鉴于百白破联合疫苗在公司销售收入总额中占比较小,因此上述事项对公司目前生产经营无重大影响。
而从公司股价上来看,虽然在百白破疫苗事件后有多日降幅,但自2018年2月以来,长生生物的总体走势仍呈上涨趋势。
与此同时,6月8日,国家药监局刚刚批准了华兰生物疫苗有限公司和长春长生生物科技股份有限公司的四价流感病毒裂解疫苗的生产注册申请。
不过,此次狂犬疫苗的停产及召回,是否会影响到该公司其他疫苗的生产,尚未得知。此外,此次国家药监局的飞检通报尚未涉及长春长生生物所生产冻干人用狂犬病疫苗是否存在效价或者质量问题。
7月15日晚,针对此事,@人民日报发表评论:连狂犬病疫苗也敢造假,既胆大包天,又伤天害理。幸亏所涉批次产品尚未上市销售,否则后果不堪设想。疫苗关涉生命安全,来不得丝毫猫腻,容不得半点瑕疵,也使不得一点侥幸。用彻查还原真相,依法处理打消公众恐慌,确保药品安全。